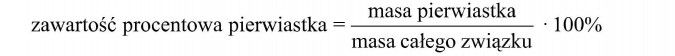zaprasza Cię do wspólnej nauki fiszek
Teksty dostarczyło Wydawnictwo GREG. © Copyright by Wydawnictwo GREG
Autorzy opracowań: B. Wojnar, B. Włodarczyk, A Sabak, D. Stopka, A Szostak, D. Pietrzyk, A. Popławska, E. Seweryn, M. Zagnińska, J. Paciorek, E. Lis, M. D. Wyrwińska, A Jaszczuk, A Barszcz, A. Żmuda, K. Stypinska, A Radek, J. Fuerst, C. Hadam, I. Kubowia-Bień, M. Dubiel, J. Pabian, M. Lewcun, B. Matoga, A. Nawrot, S. Jaszczuk, A Krzyżek, J. Zastawny, K. Surówka, E. Nowak, P. Czerwiński, G. Matachowska, B. Więsek, Z. Daszczyńska, R. Całka
Zgodnie z regulaminem serwisu www.opracowania.pl, rozpowszechnianie niniejszego materiału w wersji oryginalnej albo w postaci opracowania, utrwalanie lub kopiowanie materiału w celu rozpowszechnienia w szczególności zamieszczanie na innym serwerze, przekazywanie drogą elektroniczną i wykorzystywanie materiału w inny sposób niż dla celów własnej edukacji bez zgody autora jest niedozwolone.
Prawo stałości składu związku chemicznego sformułował J.L. Proust i brzmi ono:
Skład związku chemicznego jest zawsze stały, tzn. stosunek wagowy pierwiastków wchodzących w skład określonego związku chemicznego jest zawsze jednakowy.
Pewna ilość substancji reaguje ze ściśle określoną ilością drugiej substancji.
Każda cząsteczka składa się z określonej liczby atomów. Masa atomów jest stała i w reakcjach chemicznych nie ulega zmianie. Stosunki wagowe atomów w danej cząsteczce są stałe bez względu na metody otrzymywania danego związku.
Przeanalizujmy skład cząsteczki wody.
H2O w cząsteczce wody są dwa atomy wodoru i jeden atom tlenu.
Stosunek wagowy wodoru do tlenu w cząsteczce wody wynosi:
Stosunek wagowy wodoru do tlenu w cząsteczce wody wynosi 1 : 8.
Oznacza to, że 1 część masowa wodoru łączy się z 8 częściami masowymi tlenu i powstaje 9 części masowych wody (aby wyprodukować wodę, na każdy kilogram wodoru należy użyć osiem kilogramów tlenu, mając do dyspozycji 3 kg wodoru musimy użyć 8 razy więcej tlenu, czyli 8 · 3 kg = 24 kg tlenu).
Stosunek ilościowy pierwiastków zawartych w związku chemicznym jest zawsze stały i możemy go przedstawić jako stosunek masowy (stosunek mas atomów w cząsteczce) lub wyrazić w procentach (będzie przedstawiał zawartość procentową poszczególnych składników).
Zawartość procentowa danego pierwiastka to wyrażony w procentach stosunek masy pierwiastka w cząsteczce do masy całej cząsteczki (ułamka wagowego) pierwiastka.
Oblicz, jaki jest stosunek mas pierwiastków w tlenku żelaza (III) Fe2O3.
Odp.: Stosunek żelaza do tlenu w tlenku żelaza (III) wynosi 7 : 3 (czytamy siedem do trzech).
Pogłębiaj wiedzę w temacie: Prawo stałości składu związku chemicznego
Teksty dostarczyło Wydawnictwo GREG. © Copyright by Wydawnictwo GREG
Autorzy opracowań: B. Wojnar, B. Włodarczyk, A Sabak, D. Stopka, A Szostak, D. Pietrzyk, A. Popławska, E. Seweryn, M. Zagnińska, J. Paciorek, E. Lis, M. D. Wyrwińska, A Jaszczuk, A Barszcz, A. Żmuda, K. Stypinska, A Radek, J. Fuerst, C. Hadam, I. Kubowia-Bień, M. Dubiel, J. Pabian, M. Lewcun, B. Matoga, A. Nawrot, S. Jaszczuk, A Krzyżek, J. Zastawny, K. Surówka, E. Nowak, P. Czerwiński, G. Matachowska, B. Więsek, Z. Daszczyńska, R. Całka
Zgodnie z regulaminem serwisu www.opracowania.pl, rozpowszechnianie niniejszego materiału w wersji oryginalnej albo w postaci opracowania, utrwalanie lub kopiowanie materiału w celu rozpowszechnienia w szczególności zamieszczanie na innym serwerze, przekazywanie drogą elektroniczną i wykorzystywanie materiału w inny sposób niż dla celów własnej edukacji bez zgody autora jest niedozwolone.