zaprasza Cię do wspólnej nauki fiszek
Teksty dostarczyło Wydawnictwo GREG. © Copyright by Wydawnictwo GREG
Autorzy opracowań: B. Wojnar, B. Włodarczyk, A Sabak, D. Stopka, A Szostak, D. Pietrzyk, A. Popławska, E. Seweryn, M. Zagnińska, J. Paciorek, E. Lis, M. D. Wyrwińska, A Jaszczuk, A Barszcz, A. Żmuda, K. Stypinska, A Radek, J. Fuerst, C. Hadam, I. Kubowia-Bień, M. Dubiel, J. Pabian, M. Lewcun, B. Matoga, A. Nawrot, S. Jaszczuk, A Krzyżek, J. Zastawny, K. Surówka, E. Nowak, P. Czerwiński, G. Matachowska, B. Więsek, Z. Daszczyńska, R. Całka
Zgodnie z regulaminem serwisu www.opracowania.pl, rozpowszechnianie niniejszego materiału w wersji oryginalnej albo w postaci opracowania, utrwalanie lub kopiowanie materiału w celu rozpowszechnienia w szczególności zamieszczanie na innym serwerze, przekazywanie drogą elektroniczną i wykorzystywanie materiału w inny sposób niż dla celów własnej edukacji bez zgody autora jest niedozwolone.
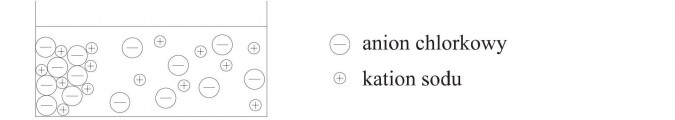
Rozpuszczanie to zjawisko fizyczne. Jest to proces mieszania się substancji rozpuszczanej (np. soli) z rozpuszczalnikiem. W czasie rozpuszczania substancja jest rozbijana na pojedyncze cząstki lub jony (cząstki obdarzone ładunkiem).
Woda jest bardzo dobrym rozpuszczalnikiem dla wielu substancji. Do substancji dobrze rozpuszczających się w wodzie należy np. sól, cukier. Tworzą one z wodą mieszaniny jednorodne, które nazywamy roztworami.
W mieszaninie jednorodnej składników mieszaniny nie widać gołym okiem.
Roztwór = substancja rozpuszczana + rozpuszczalnik
Ze względu na wielkość cząsteczek substancji rozpuszczanej roztwory dzielimy na:
- Roztwory właściwe - cząsteczki są mniejsze od jednej stumilionowej milimetra. Wiązka światła przechodzi przez roztwór właściwy bez problemu, dlatego jej nie widzimy. Cząsteczki substancji rozpuszczanej są zbyt małe, aby rozpraszać światło. Przykładem roztworu właściwego jest roztwór wody i cukru.
- Roztwory koloidalne - cząsteczki w tym roztworze mają rozmiary od jednej milionowej do pięciu stumilionowych milimetra. Cząsteczki substancji rozpuszczanej są na tyle duże, że rozpraszają promień światła przechodzący przez roztwór koloidalny i dlatego jest on dla nas widoczny. Rozproszenie promienia światła na cząstkach roztworu koloidalnego nazywamy efektem Tyndalla. Przykładem roztworu koloidalnego jest kleik skrobiowy, czyli mąka rozpuszczona w gorącej wodzie.
Przy roztworach omawia się również układy niejednorodne, zwane zawiesinami. W zawiesinach cząsteczki są większe od pięciu stumilionowych milimetra. Przykładem zawiesiny jest mąka z zimną wodą, rozdrobniona kreda z wodą.
Ze względu na ilość rozpuszczonej substancji wyróżniamy:
- Roztwór nasycony - w określonej temperaturze w danej objętości wody nie można już rozpuścić więcej substancji (dodawana substancja pozostaje w roztworze nie rozpuszczona).
- Roztwór nienasycony - w określonej temperaturze w danej objętości wody można jeszcze rozpuścić pewną ilość substancji.
Wśród roztworów nienasyconych wyróżniamy:
- Roztwór stężony - ilość substancji rozpuszczonej jest większa w stosunku do ilości wody.
- Roztwór rozcieńczony - ilość substancji rozpuszczonej jest mała w stosunku do ilości wody.
Pogłębiaj wiedzę w temacie: Woda jako rozpuszczalnik (rodzaje roztworów)
Teksty dostarczyło Wydawnictwo GREG. © Copyright by Wydawnictwo GREG
Autorzy opracowań: B. Wojnar, B. Włodarczyk, A Sabak, D. Stopka, A Szostak, D. Pietrzyk, A. Popławska, E. Seweryn, M. Zagnińska, J. Paciorek, E. Lis, M. D. Wyrwińska, A Jaszczuk, A Barszcz, A. Żmuda, K. Stypinska, A Radek, J. Fuerst, C. Hadam, I. Kubowia-Bień, M. Dubiel, J. Pabian, M. Lewcun, B. Matoga, A. Nawrot, S. Jaszczuk, A Krzyżek, J. Zastawny, K. Surówka, E. Nowak, P. Czerwiński, G. Matachowska, B. Więsek, Z. Daszczyńska, R. Całka
Zgodnie z regulaminem serwisu www.opracowania.pl, rozpowszechnianie niniejszego materiału w wersji oryginalnej albo w postaci opracowania, utrwalanie lub kopiowanie materiału w celu rozpowszechnienia w szczególności zamieszczanie na innym serwerze, przekazywanie drogą elektroniczną i wykorzystywanie materiału w inny sposób niż dla celów własnej edukacji bez zgody autora jest niedozwolone.