zaprasza Cię do wspólnej nauki fiszek
Teksty dostarczyło Wydawnictwo GREG. © Copyright by Wydawnictwo GREG
Autorzy opracowań: B. Wojnar, B. Włodarczyk, A Sabak, D. Stopka, A Szostak, D. Pietrzyk, A. Popławska, E. Seweryn, M. Zagnińska, J. Paciorek, E. Lis, M. D. Wyrwińska, A Jaszczuk, A Barszcz, A. Żmuda, K. Stypinska, A Radek, J. Fuerst, C. Hadam, I. Kubowia-Bień, M. Dubiel, J. Pabian, M. Lewcun, B. Matoga, A. Nawrot, S. Jaszczuk, A Krzyżek, J. Zastawny, K. Surówka, E. Nowak, P. Czerwiński, G. Matachowska, B. Więsek, Z. Daszczyńska, R. Całka
Zgodnie z regulaminem serwisu www.opracowania.pl, rozpowszechnianie niniejszego materiału w wersji oryginalnej albo w postaci opracowania, utrwalanie lub kopiowanie materiału w celu rozpowszechnienia w szczególności zamieszczanie na innym serwerze, przekazywanie drogą elektroniczną i wykorzystywanie materiału w inny sposób niż dla celów własnej edukacji bez zgody autora jest niedozwolone.
Grafit, diament, fullereny to odmiany węgla, różniące się rozmieszczeniem atomów węgla w sieci krystalicznej - to znaczy, że w każdej z tych odmian atomy węgla są ze sobą inaczej „połączone”.
Takie odmiany nazywamy alotropowymi.
Różnice w budowie sieci krystalicznej powodują różnice we właściwościach fizycznych tych substancji.
Niektóre własności fizyczne podaje tabela:
| Grafit | Diament | Fulleren |
|---|---|---|
|
|
|
Porównując dane w tabeli widzimy, że odmiany alotropowe węgla różnią się między innymi:
- stopniem przezroczystości
- barwą
- twardością
- przewodnictwem elektryczności.
- przezroczysty diament, półprzezroczysty fulleren, nieprzezroczysty grafit
- różne barwy
- najtwardszy z minerałów - diament oraz bardzo miękki - grafit
- diament nie przewodzi prądu elektrycznego, grafit przewodzi prąd, półprzewodnikowe i nadprzewodnikowe własności fullerenu
Grafit
Diament
Jeden z elementów sieci krystalicznej diamentu.
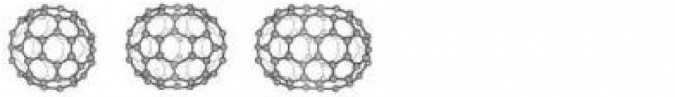
Fulleren
Atomy węgla w fullerenach łączą się ze sobą, tworząc kryształy o różnym kształcie.
Zapamiętaj!
1. Węgiel to ważny składnik całej przyrody ożywionej.
2. Węgiel występuje w przyrodzie w stanie wolnym jako: grafit, diament, fulleren oraz w postaci związków chemicznych: w skałach, minerałach, jako składnik przyrody ożywionej.
3. Odmiany alotropowe węgla mają różną budowę wewnętrzną sieci krystalicznej. Inna budowa wewnętrzna, czyli inny sposób „połączeń” między atomami węgla, wpływa na różnice we własnościach fizycznych: grafitu, diamentu czy fullerenów.
Pogłębiaj wiedzę w temacie: Odmiany alotropowe węgla
Teksty dostarczyło Wydawnictwo GREG. © Copyright by Wydawnictwo GREG
Autorzy opracowań: B. Wojnar, B. Włodarczyk, A Sabak, D. Stopka, A Szostak, D. Pietrzyk, A. Popławska, E. Seweryn, M. Zagnińska, J. Paciorek, E. Lis, M. D. Wyrwińska, A Jaszczuk, A Barszcz, A. Żmuda, K. Stypinska, A Radek, J. Fuerst, C. Hadam, I. Kubowia-Bień, M. Dubiel, J. Pabian, M. Lewcun, B. Matoga, A. Nawrot, S. Jaszczuk, A Krzyżek, J. Zastawny, K. Surówka, E. Nowak, P. Czerwiński, G. Matachowska, B. Więsek, Z. Daszczyńska, R. Całka
Zgodnie z regulaminem serwisu www.opracowania.pl, rozpowszechnianie niniejszego materiału w wersji oryginalnej albo w postaci opracowania, utrwalanie lub kopiowanie materiału w celu rozpowszechnienia w szczególności zamieszczanie na innym serwerze, przekazywanie drogą elektroniczną i wykorzystywanie materiału w inny sposób niż dla celów własnej edukacji bez zgody autora jest niedozwolone.