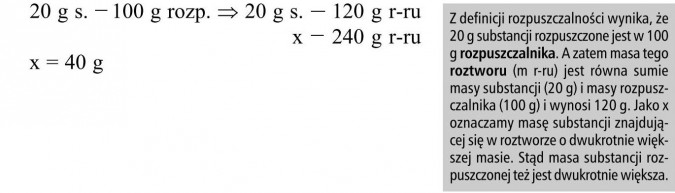zaprasza Cię do wspólnej nauki fiszek
Teksty dostarczyło Wydawnictwo GREG. © Copyright by Wydawnictwo GREG
Autorzy opracowań: B. Wojnar, B. Włodarczyk, A Sabak, D. Stopka, A Szostak, D. Pietrzyk, A. Popławska, E. Seweryn, M. Zagnińska, J. Paciorek, E. Lis, M. D. Wyrwińska, A Jaszczuk, A Barszcz, A. Żmuda, K. Stypinska, A Radek, J. Fuerst, C. Hadam, I. Kubowia-Bień, M. Dubiel, J. Pabian, M. Lewcun, B. Matoga, A. Nawrot, S. Jaszczuk, A Krzyżek, J. Zastawny, K. Surówka, E. Nowak, P. Czerwiński, G. Matachowska, B. Więsek, Z. Daszczyńska, R. Całka
Zgodnie z regulaminem serwisu www.opracowania.pl, rozpowszechnianie niniejszego materiału w wersji oryginalnej albo w postaci opracowania, utrwalanie lub kopiowanie materiału w celu rozpowszechnienia w szczególności zamieszczanie na innym serwerze, przekazywanie drogą elektroniczną i wykorzystywanie materiału w inny sposób niż dla celów własnej edukacji bez zgody autora jest niedozwolone.
Proces polegający na mieszaniu się co najmniej dwóch substancji, w wyniku czego powstaje roztwór, nazywamy rozpuszczaniem.
Maksymalną ilość gramów substancji, którą możemy rozpuścić w 100 g rozpuszczalnika (w danej temperaturze) nazywamy rozpuszczalnością, otrzymujemy wtedy roztwór nasycony.
Np. rozpuszczalność jodku potasu w temperaturze 293 K wynosi 145 g (zapisujemy: 145 g s/100 g wody). Oznacza to, że 145 g substancji (KI) rozpuszczona jest w 100 g rozpuszczalnika. A zatem na masę całego roztworu składa się masa substancji rozpuszczonej i masa rozpuszczalnika (mr-ru = ms + mrozp.), tj. 145 g s. + 100 g rozp. = 245 g r-ru.
Zależność rozpuszczalności danej substancji od temperatury przedstawia się w formie odpowiednich wykresów, tzw. krzywych rozpuszczalności, lub zestawia w postaci danych liczbowych w tabeli.
Na podstawie krzywych rozpuszczalności możemy określić rozpuszczalność substancji w danej temperaturze oraz wykonywać obliczenia potrzebne przy sporządzaniu roztworów.
Np.: Który ze związków: NaCl czy KCl ma większą rozpuszczalność w temperaturze 90°C.
Na wykresie krzywych rozpuszczalności NaCl i KCl szukamy wartości rozpuszczalności dla podanych związków w temperaturze 90°C.
Rozpuszczalność NaCl w 90°C wynosi 42 g/100 g H2O, a KCl 56 g/100 g H2O. Oznacza to, że w temperaturze 90°C w 100 g rozpuszczalnika rozpuści się 56 g KCl i tylko 42 g NaCl. A zatem większą rozpuszczalność ma KCl.
Szybkość rozpuszczania substancji zależy od:
- rodzaju substancji rozpuszczanej
- rodzaju rozpuszczalnika
- stopnia rozdrobnienia substancji
- mechanicznego mieszania składników
- temperatury (na ogół wzrasta ze wzrostem temperatury)
Rozpuszczalność substancji zależy od:
- temperatury - rozpuszczalność cieczy i ciał stałych w cieczach na ogół wzrasta ze wzrostem temperatury, a gazów maleje
- ciśnienia w przypadku gazów - rozpuszczalność gazów w cieczach wzrasta ze wzrostem ciśnienia
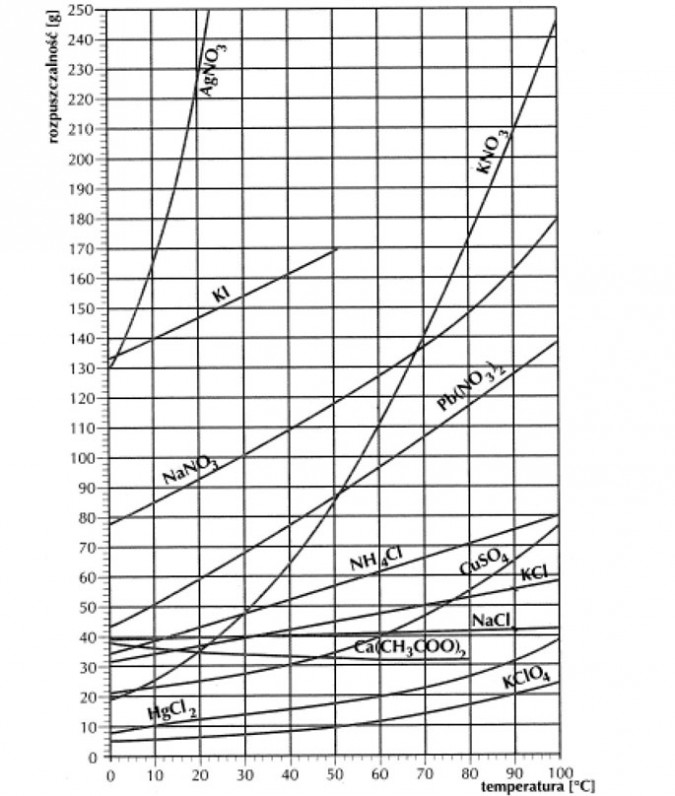
Zależność rozpuszczalności ciał stałych od temperatury (krzywe rozpuszczalności)
AgNO3 - azotan (V) srebra (I)
KI - jodek potasu
NaNO3 - azotan (V) sodu
KNO3 - azotan (V) potasu
Pb(NO3)2 - azotan (V) ołowiu (II)
NH4Cl - chlorek amonu
CuSO4 - siarczan (VI) miedzi (II)
KCl - chlorek potasu
NaCl - chlorek sodu
Ca(CH3COO)2 - octan wapnia
HgCl2 - chlorek rtęci (II)
KClO4 - chlorek (VII) potasu
Roztwór nasycony - roztwór, który pozostaje w stanie równowagi z osadem substancji rozpuszczanej. Jego oziębienie powoduje wytrącenie się z niego kryształków substancji rozpuszczonej. Proces ten nosi nazwę krystalizacji.
Roztwór nienasycony - roztwór, w którym nie ma równowagi ciecz - osad (osad substancji rozpuszczanej ulega rozpuszczeniu), ponieważ w rozpuszczalniku zostaje rozpuszczona mniejsza ilość substancji niż wynika to z jej rozpuszczalności w danych warunkach.
Rozpuszczalność azotanu (V) potasu w temperaturze 343 K wynosi 135 g. Ile gramów tej soli można rozpuścić w 300 g rozpuszczalnika w temperaturze 343 K?
Rozwiązanie:
Odp.: W 300 g rozpuszczalnika w temperaturze 343 K można rozpuścić 405 g azotanu (V) potasu.
Ile gramów substancji rozpuszczonej znajduje się w 240 g nasyconego roztworu, jeśli rozpuszczalność w tej temperaturze wynosi 20 g?
Rozwiązanie:
Odp.: W 240 g nasyconego roztworu znajduje się 40 g rozpuszczonej substancji.
Ile wody zawiera 0,5 kg roztworu nasyconego, jeśli rozpuszczalność w tej temperaturze wynosi 60 g?
Rozwiązanie:
Odp.: 0,5 kg nasyconego roztworu o rozpuszczalności 60 g zawiera 312,5 g wody (rozpuszczalnika).
Ile gramów jodku potasu (KI) należy rozpuścić w 100 g wody w temperaturze 10°C, aby otrzymać roztwór nasycony?
Rozwiązanie:
Z wykresu krzywej rozpuszczalności wynika, że w temperaturze 10°C rozpuszczalność KI wynosi 140 g, oznacza to, że w 100 g rozpuszczalnika należy rozpuścić 140 g jodku potasu, aby otrzymać roztwór nasycony (masa substancji rozpuszczonej w danej temperaturze musi być równa jej rozpuszczalności w danym rozpuszczalniku, aby otrzymany roztwór był roztworem nasyconym).
Pogłębiaj wiedzę w temacie: Rozpuszczanie i krystalizacja
Teksty dostarczyło Wydawnictwo GREG. © Copyright by Wydawnictwo GREG
Autorzy opracowań: B. Wojnar, B. Włodarczyk, A Sabak, D. Stopka, A Szostak, D. Pietrzyk, A. Popławska, E. Seweryn, M. Zagnińska, J. Paciorek, E. Lis, M. D. Wyrwińska, A Jaszczuk, A Barszcz, A. Żmuda, K. Stypinska, A Radek, J. Fuerst, C. Hadam, I. Kubowia-Bień, M. Dubiel, J. Pabian, M. Lewcun, B. Matoga, A. Nawrot, S. Jaszczuk, A Krzyżek, J. Zastawny, K. Surówka, E. Nowak, P. Czerwiński, G. Matachowska, B. Więsek, Z. Daszczyńska, R. Całka
Zgodnie z regulaminem serwisu www.opracowania.pl, rozpowszechnianie niniejszego materiału w wersji oryginalnej albo w postaci opracowania, utrwalanie lub kopiowanie materiału w celu rozpowszechnienia w szczególności zamieszczanie na innym serwerze, przekazywanie drogą elektroniczną i wykorzystywanie materiału w inny sposób niż dla celów własnej edukacji bez zgody autora jest niedozwolone.