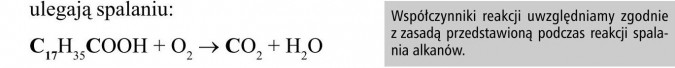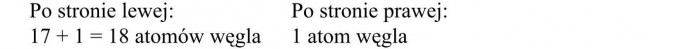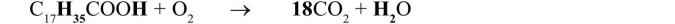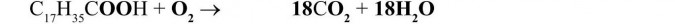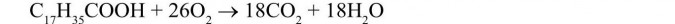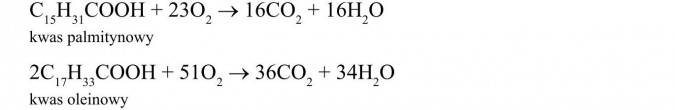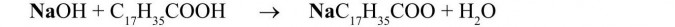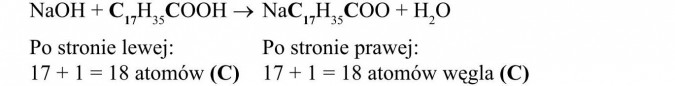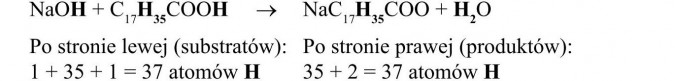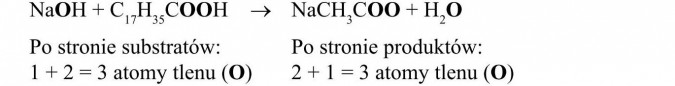zaprasza Cię do wspólnej nauki fiszek
Teksty dostarczyło Wydawnictwo GREG. © Copyright by Wydawnictwo GREG
Autorzy opracowań: B. Wojnar, B. Włodarczyk, A Sabak, D. Stopka, A Szostak, D. Pietrzyk, A. Popławska, E. Seweryn, M. Zagnińska, J. Paciorek, E. Lis, M. D. Wyrwińska, A Jaszczuk, A Barszcz, A. Żmuda, K. Stypinska, A Radek, J. Fuerst, C. Hadam, I. Kubowia-Bień, M. Dubiel, J. Pabian, M. Lewcun, B. Matoga, A. Nawrot, S. Jaszczuk, A Krzyżek, J. Zastawny, K. Surówka, E. Nowak, P. Czerwiński, G. Matachowska, B. Więsek, Z. Daszczyńska, R. Całka
Zgodnie z regulaminem serwisu www.opracowania.pl, rozpowszechnianie niniejszego materiału w wersji oryginalnej albo w postaci opracowania, utrwalanie lub kopiowanie materiału w celu rozpowszechnienia w szczególności zamieszczanie na innym serwerze, przekazywanie drogą elektroniczną i wykorzystywanie materiału w inny sposób niż dla celów własnej edukacji bez zgody autora jest niedozwolone.
Sprawdzamy liczbę atomów węgla po obu stronach reakcji:
Aby było równo po obu stronach - stronę prawą należy pomnożyć przez 18. W reakcji chemicznej piszemy więc 18 przed związkiem zawierającym węgiel czyli przed tlenkiem węgla IV. Mamy więc:
Teraz chcemy sprawdzić liczbę atomów wodoru po obu stronach równania reakcji chemicznej:
Aby było tyle samo atomów wodoru po obu stronach, należy stronę prawą pomnożyć przez 18. Po stronie prawej musimy więc wpisać 18 przed wzorem chemicznym związku, w którym znajduje się wodór, tj. przed wodą.
Mamy więc:
Pozostały więc do sprawdzenia tylko atomy tlenu po obu stronach równania:
Mamy więc:
Postępując identycznie jak w poprzednim przypadku, możemy napisać reakcje spalania pozostałych kwasów:
Kwas oleinowy odbarwia wodę bromową i manganian VII potasu, co oznacza, że łańcuch węglowodorowy tego kwasu zawiera wiązanie wielokrotne (podwójne).
Kwasy tłuszczowe reagują z wodorotlenkiem sodu lub potasu. W czasie tej reakcji powstają sole, zwane mydłami. Mydła znalazły zastosowanie jako środki myjące i piorące.
Równanie zachodzącej reakcji ma postać:
Sól, która powstała w tej reakcji będzie nazwana od kwasu, z którego powstała (od kwasu styrenowego) - stearynianem sodu.
Sprawdzamy teraz, czy równanie reakcji otrzymywania stearynianu sodu zostało napisane poprawnie, tzn. czy ilość atomów Na, C, H, O po stronie substratów jest taka sama jak po stronie produktów:
sprawdzamy atomy sodu:
Jest więc w porządku, bo po obu stronach jest tyle samo atomów sodu.
- sprawdzamy atomy węgla:
Liczba atomów węgla zgadza się po obu stronach równania reakcji. Nie musimy więc dopasowywać współczynników stechiometrycznych.
- sprawdzamy atomy H - wodoru:
Liczba atomów wodoru po obu stronach jest taka sama.
- sprawdzamy teraz atomy tlenu (O)
Liczba atomów tlenu po obu stronach jest taka sama, a więc reakcja otrzymywania stearynianu sodu jest napisana prawidłowo.
Pogłębiaj wiedzę w temacie: Własności chemiczne wyższych kwasów karboksylowych
Teksty dostarczyło Wydawnictwo GREG. © Copyright by Wydawnictwo GREG
Autorzy opracowań: B. Wojnar, B. Włodarczyk, A Sabak, D. Stopka, A Szostak, D. Pietrzyk, A. Popławska, E. Seweryn, M. Zagnińska, J. Paciorek, E. Lis, M. D. Wyrwińska, A Jaszczuk, A Barszcz, A. Żmuda, K. Stypinska, A Radek, J. Fuerst, C. Hadam, I. Kubowia-Bień, M. Dubiel, J. Pabian, M. Lewcun, B. Matoga, A. Nawrot, S. Jaszczuk, A Krzyżek, J. Zastawny, K. Surówka, E. Nowak, P. Czerwiński, G. Matachowska, B. Więsek, Z. Daszczyńska, R. Całka
Zgodnie z regulaminem serwisu www.opracowania.pl, rozpowszechnianie niniejszego materiału w wersji oryginalnej albo w postaci opracowania, utrwalanie lub kopiowanie materiału w celu rozpowszechnienia w szczególności zamieszczanie na innym serwerze, przekazywanie drogą elektroniczną i wykorzystywanie materiału w inny sposób niż dla celów własnej edukacji bez zgody autora jest niedozwolone.